펩티드 유사 합성 기술
펩티드 약물의 연구 및 개발은 의학에서 빠르게 성장하고 있습니다. 그러나, 펩티드 약물의 발달은 자체 특성에 의해 제한된다. 예를 들어, 효소 가수 분해에 대한 특수 민감도로 인해 안정성이 감소되고 입체 형태의 변동성은 낮은 표적화 특이성, 낮은 소수성 및 특정 전송 시스템의 부족을 초래합니다. 이들 펩티드를 극복하기 위해, 많은 용액을 제안하고 한 종류의 펩티드의 성공적인 적용이 그 중 하나입니다.
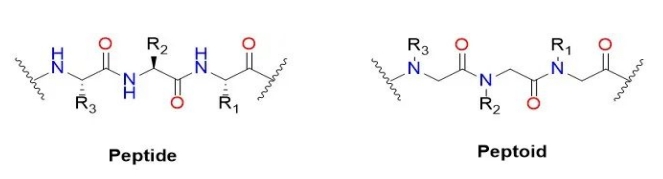
글리신 대신 펩티드의 종류 (영어 이름 : 펩타이드) 또는 폴리 - N - (영어 이름 : 폴리 real - n - 치환 글리신), 그것은 주 사슬에서 펩티드의 준 펩티드 화합물입니다. 알파 탄소 측쇄는 측쇄 대신 주 사슬 질소를 전달합니다. 원래의 폴리펩티드에서, 아미노산 측쇄의 R 그룹은 20 개의 상이한 아미노산을 나타내지 만, R 그룹은 펩타이드에서 더 많은 옵션을 갖는다. 펩티드에서, 전 사슬로 전달되는 대신 알파 탄소 질소의 아미노산의 주간의 펩티드. 펩티드는 일반적으로 골격 질소의 수소 부족으로 인해 펩티드 및 단백질의 2 차 구조와 동일한 고급 순서 구조를 생성하지 않는다는 점을 언급 할 가치가있다. 펩티드 초기 목적은 소분자 약물의 안정적인 프로테아제 펩티드를 개발하는 것입니다.
펩티드-유사 합성 기술의 분석
펩티드 합성 방법이 도입되었다
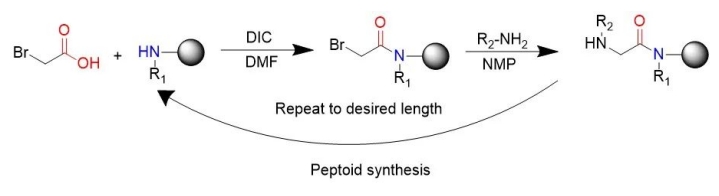
일반적으로 인기있는 펩티드-유사 합성 방법은 Ronzuckermann에 의해 발명 된 서브 단일 합성 방법이며, 각각은 아실화 및 변위의 두 단계로 나뉩니다. 아실화에서, 첫 번째 단계는 후광산을 활성화하여 이전 단계의 끝에 남아있는 아민과 반응하는 것입니다. Bromoaceticacid는 Diisopropylcarbodiimide에 의해 활성화되었다. "치환 반응 (이질성 친 핵성 치환 반응)에서, 전형적으로 1 차 아민은 대안적인 할로겐을 공격하여 n- 치환 된 글리신을 형성한다." 하위 유방 합성 경로는 쉽게 이용 가능한 1 차 아민을 사용하여 펩티드를 생성함으로써 펩티드의 화학적 합성을 가능하게한다.
클래스 펩티드 합성의 고체 연장은 풍부한 경험을 가지며 다양한 종류의 펩티드 합성 서비스를 제공 할 수 있습니다.
펩티드-유사 합성 기술의 분석
이러한 펩티드의 장점
더 안정적 : 펩 토이드는 펩티드보다 생체 내에서 더 안정적이다.
더 많은 선택성 : 펩타이드는 백본 아미노기의 변형에 의해 다양한 폴리펩티드 빌딩 블록이 얻을 수 있기 때문에 결합 된 약물 발견 연구에 적합하다.
보다 효율적인 : 펩 토이 토이드 구조의 풍부함은 펩 토이드를 스캐닝 방법론에 단백질에 결합하는 특정 구조를 신속하게 찾을 수 있도록 선택할 수 있습니다.
더 많은 시장 잠재력 : 펩티드의 종류의 특성은 일종의 약물 개발이 될 수있는 잠재력이 큰 잠재력을 가지고 있습니다.
후 시간 : 2025-07-02