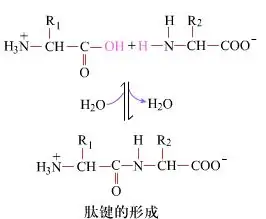
표면적으로, 디 펩티드를 생성하는 펩티드 결합의 형성은 간단한 화학적 과정이다. 이는 두 아미노산 성분이 탈수되는 동안 펩티드 결합, 아미드 결합에 의해 연결됨을 의미한다.
펩티드 결합 형성은 가벼운 반응 조건 하에서 아미노산의 활성화이다. (A) 카르 복실 부분, 제 2 아미노산 (B) 친 핵성 활성화 된 카르 복실 부분은 디 펩티드 (A-B)를 형성한다. "카르 복실 성분 (A)이 보호되지 않으면 펩티드 결합의 형성을 제어 할 수 없습니다." 선형 및 사이 클릭 펩티드와 같은 부산물은 표적 화합물 A-B와 혼합 될 수있다. 따라서, 펩티드 결합 형성에 관여하지 않은 모든 기능 그룹은 펩티드 합성 동안 일시적으로 가역적으로 보호되어야한다.
따라서, 각각의 펩티드 결합의 형성 인 펩티드 합성은 3 단계의 응집을 포함한다.
첫 번째 단계는 보호가 필요한 일부 아미노산을 준비하는 것입니다. 아미노산의 양쪽 이온 성 구조는 더 이상 존재하지 않습니다.
두 번째 단계는 펩티드 결합을 형성하기위한 2 단계 반응으로, N- 보호 된 아미노산의 카르 복실 그룹이 먼저 활성 중간체로 활성화되고 펩티드 결합이 형성된다. 이 결합 된 반응은 1 단계 반응 또는 2 개의 순차적 반응으로서 발생할 수있다.
세 번째 단계는 보호베이스의 선택적 제거 또는 완전한 제거입니다. 모든 제거는 모든 펩티드 사슬이 조립 된 후에 만 발생할 수 있지만, 펩티드 합성을 계속하기 위해서는 보호 기의 선택적 제거가 필요하다.
10 개의 아미노산 (SER, THR, TYR, ASP, GLU, LYS, ARG, HIS, SEC 및 CYS)에는 선택적 보호가 필요한 측쇄 기능 그룹이 포함되어 펩티드 합성이 더욱 복잡해집니다. 선택성에 대한 요구 사항이 다르기 때문에 임시 및 반영구 보호 기반을 구별해야합니다. 임시 보호 그룹은 다음 단계에서 아미노산 또는 카르 복실 기능 그룹의 임시 보호를 반영하기 위해 사용된다. 반 영구적 인 보호 그룹은 이미 형성된 펩티드 결합 또는 아미노산 측쇄, 때로는 합성 동안 제거됩니다.
"이상적으로, 카르 복실 성분의 활성화 및 후속 펩티드 결합 (커플 링 반응)의 형성은 라 세미 또는 부산물 형성없이 빠르야하며, 높은 수율을 달성하기 위해 어금니 반응물을 적용해야한다." 불행히도, 화학적 커플 링 방법 중 어느 것도 이러한 요구 사항을 충족하지 않으며 실제 합성에 적합한 사람은 거의 없습니다.
펩티드 합성 동안, 다양한 반응에 관여하는 기능 그룹은 일반적으로 수동 센터와 연결되어 있고, 글리신은 유일한 예외이며, 회전의 잠재적 위험이있다.
펩티드 합성 사이클의 마지막 단계는 모든 보호 그룹의 제거입니다. 보호 그룹의 선택적 제거는 디 펩티드 합성에서의 보호의 완전한 제거 요구 사항 외에 펩티드 사슬 확장에 중요하다. 합성 전략을 신중하게 계획해야합니다. 전략적 선택에 따라 N은 α- 아미노 또는 카르 복실 보호 그룹을 선택적으로 제거 할 수 있습니다. "전략"이라는 용어는 개별 아미노산의 응축 반응 순서를 나타냅니다. 일반적으로 점진적인 합성과 조각 응축 사이에는 차이가 있습니다. 펩티드 합성 ( "기존 합성"이라고도 함)은 용액에서 발생합니다. 대부분의 경우, 펩티드 사슬을 사용하여 짧은 단편을 합성함으로써 펩티드 사슬의 점진적인 연장은 합성 될 수있다. 더 긴 펩티드를 합성하기 위해, 표적 분자는 적절한 단편으로 분류되어야하고 C 말단에서 분화 정도를 최소화 할 수 있다고 결정해야한다. 개별 단편이 점차 조립 된 후, 표적 화합물이 결합 될 것이다. 펩티드 합성의 전략은 가장 적합하고 가장 적절한 보호 단편의 선택을 포함하고, 펩티드 합성의 전략은 보호 염기의 가장 적절한 조합의 선택과 단편 컨쥬 게이션의 최상의 방법을 포함한다.
후 시간 : 2025-07-02