아미노산은 무엇입니까?
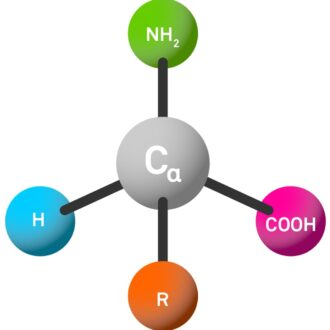
본질적으로 가장 흔한 아미노산을 α- 아미노산이라고합니다. 이 분자들은 중심 탄소 원자에 부착 된 4 개의 상이한 치환기 (α-C 원자라고 함)를 갖는다 :
아미노 (NH₂, 3 글자 코드는 "H-"로 약칭).
카르 복실 산 그룹 (COOH, 3 글자 코드에서 "-oh"로 약칭).
측쇄(R은 매우 가변적이며 아미노산의 특성과 최종 펩티드를 결정합니다).
수소 원자 (시간).
α-C 원자를 이들 4 개의 다른 그룹과 연결하면 독특한 화학적 특성을 제공하며, 이는 아미노산 및 펩티드의 거동과 특성을 결정하는 데 중요한 역할을한다.
아미노산의 생물학적 활성
아미노산은 다음과 같은 생물학적 활성을 나타낼 수 있습니다.
Tryptophan (TRP)과 Glutamic Acid (GLU)는 대사 과정에서 중요한 역할을합니다.
R 그룹 (또는 측쇄)은 아미노산의 고유 한 특성을 결정합니다. 이 그룹은 다음과 같습니다.
간단히 :글리신 (Gly)과 같은 수소 원자.
기타 산이 포함됩니다. 예를 들어 아스파르트 산 (ASP) 및 글루탐산 (GLU)과 같은.
기본 그룹 휴대 :아르기닌 (ARG), 라이신 (LYS) 또는 히스티딘 (HIS).
극 그룹이 포함되어 있습니다. 세린 (Ser) 또는 트레오닌 (THR)과 같은.
비극성 탄화수소 :알라닌 (ALA), 페닐알라닌 (PHE) 또는 발린 (VAL).
황 함량 :시스테인 (CYS) 및 메티오닌 (MET)에서 볼 수 있듯이.
L- 아미노산 및 D- 아미노산의 역할
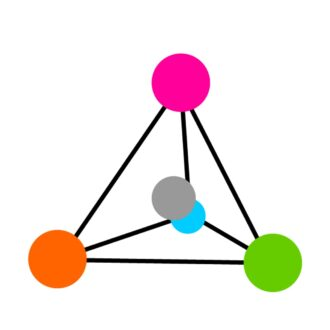
α-C 원자의 4 개의 치환기는 사면체의 모서리에 배열되며, α-C 원자는 중심에있다 (도 3 참조). 이 배열은 두 가지 형태의 아미노산 분자가 왼쪽과 오른손과 유사하게 거울 형태로 존재할 수있게한다. 이 거울 형태는 "입체 이성질체"또는 "거울상 이성질체"로 알려져 있습니다.
거울상 이성질체의 생물학적 중요성
거울상 이성질체는 거의 동일한 화학적 및 물리적 특성을 가지고 있지만, 이들의 생물학적 효과는 크게 다를 수있다. 분자 모양은 생물학적 표적과의 상호 작용에 중요합니다. 한 거울상 이성질체는 표적에 효과적으로 결합 할 수 있으며, 다른 경우 다른 경우에는 부정적인 영향을 미치지 않을 수 있습니다. 용액에서, 거울상 이성질체는 반대 방향으로 편광 평면을 회전시킨다.
후 시간 : 2025-09-05
